合成生物学驱动新质生产力
最近“新质生产力”爆火!“生物制造”也成为热搜名词!新质生产力是什么?生物制造又是什么?两者有什么联系?跟着小编来一探究竟~

什么是新质生产力?
新质生产力是由技术革命性突破、生产要素创新性配置、产业深度转型升级而催生的当代先进生产力。其特点是创新,关键在优质,本质是先进生产力。
2024年政府工作报告中指出 “加快前沿新兴氢能、新材料、创新药等产业发展, 积极打造生物制造、商业航天、低空经济等新增长引擎”。其中,生物制造作为生物技术领域的重要分支,正逐渐成为推动经济增长和产业升级的重要力量。
什么是生物制造?
生物制造是一种利用生物系统(如微生物、动植物、酶或体外合成酶系统)来生产在农业、食品、材料、能源和制药行业中具有商业重要性的生物分子的生产方式。生物制造作为新质生产力和战略性新兴产业的重要方向之一,正在逐步成为先进制造业的核心构成。
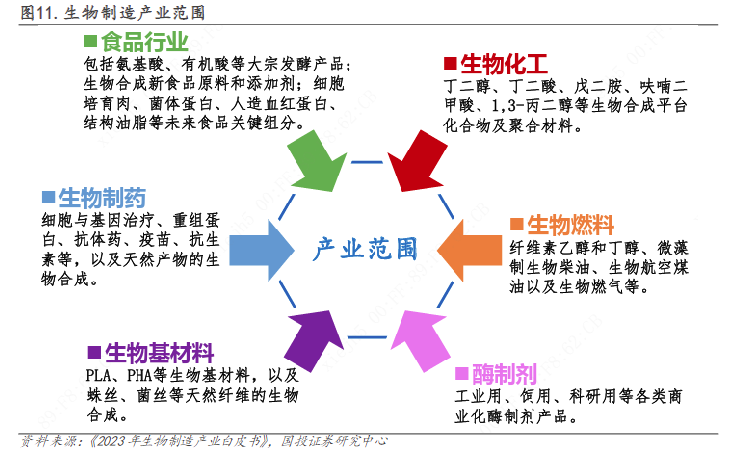
生物制造平台根据生物催化剂种类可以分为基于细胞工厂的微生物发酵、基于酶分子的生物催化和基于多酶分子机器的体外生物转化。
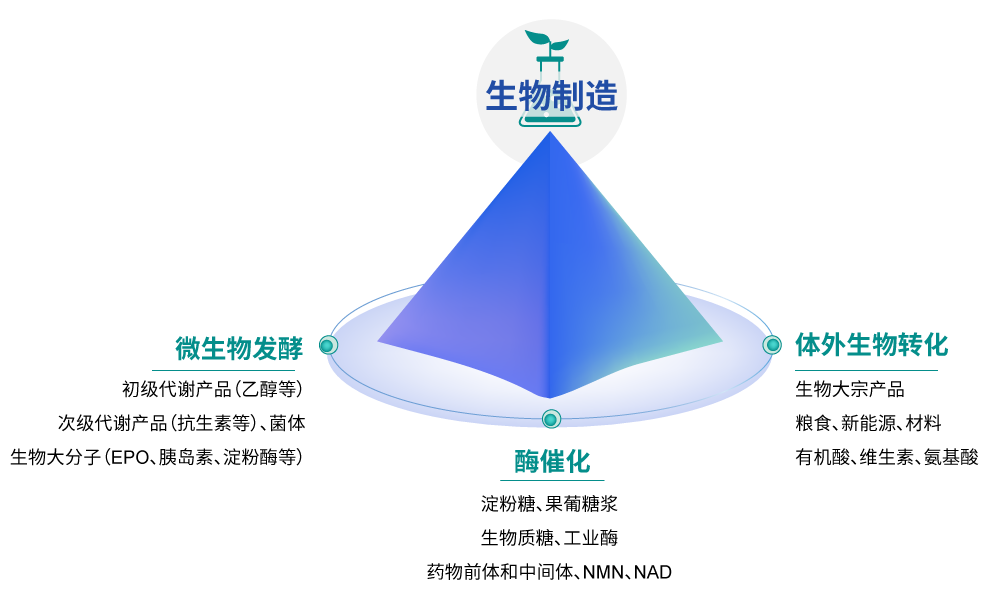
合成生物学——底层技术进步推动生物制造成本降低
合成生物学通过设计和构建新的人工生物途径或改造现有自然生物系统,来解决人类面临的食品缺乏、能源紧缺、环境污染、医疗健康等问题。合成生物学的技术逻辑基于DBTL(设计-构建-测试-学习)的循环迭代过程。在生物制造方向,其目的是持续提升微生物性能,打破最终产物的生产瓶颈。
过去获取高产菌种主要依赖于筛选和诱变育种的方式,这种“以时间或人力换水平”的非理性策略,耗时且效率低。随着基因测序、基因合成、基因编辑等关键底层技术进步和成本的不断降低,研究人员对DNA、RNA、蛋白质和细胞表型的设计和改造能力显著提升。通过工程化手段,可更精确地构建微生物工厂,更高效的生产出所需产物。
这种合成生物制造的方式不仅提高了生产效率和产物的质量,还降低了生产成本,为各个行业带来新的发展机遇!
生物医药领域
2006年4月, Jay Keasling的团队成功地在面包酵母中构建了青篙酸的生物合成途径,使其产生出100毫克/升的青篙酸。通过基因编辑和基因表达调控等技术,对酵母中MVA途径代谢调控关系的调整,关键基因表达量的优化,前提物FPP代谢支路的削弱,结合氧化酶CYP71AV1的表达,研究团队成功构建生产青篙酸的酵母菌株。
改造后的“生物工厂”重建了青篙素的生物合成途径,能够高效地将简单的碳源转化为青篙酸,从而提高青篙素的生产效率和产量。为之后研究青篙素半合成(微生物合成+化学合成)重大突破打下基础。2013年,世界卫生组织批准微生物合成的青篙素作为临床药物使用。这种药物微生物生产成本降到了从植物中提取的十分之一。

从烧瓶中的酵母到40吨青篙素药物,通过生物制造生产青篙素是合成生物学在现实世界中第一个重大成就。
传统的生产方法依赖于从青篙植物中提取,这受限于植物生长周期、产量和提取效率。随着合成生物学的发展,科学家们开始利用合成生物学技术,通过生物制造的方式生产青篙素。
基因“读”、“写”、“编”底层技术为生物制造青篙素提供了强有力的支持,为全球抗击疟疾提供了稳定、高效的药物来源。这些技术的应用展示了合成生物学在生物医药领域的巨大潜力和广阔前景。

医美领域
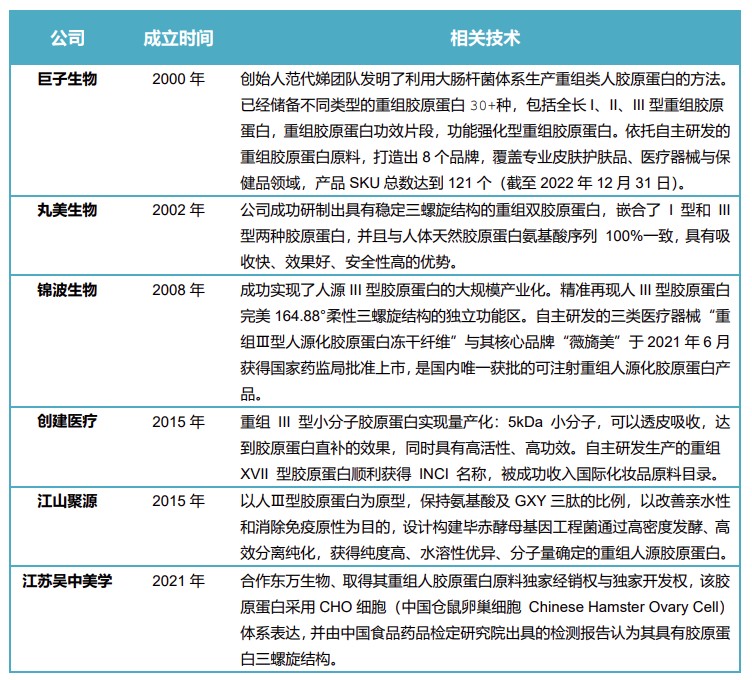
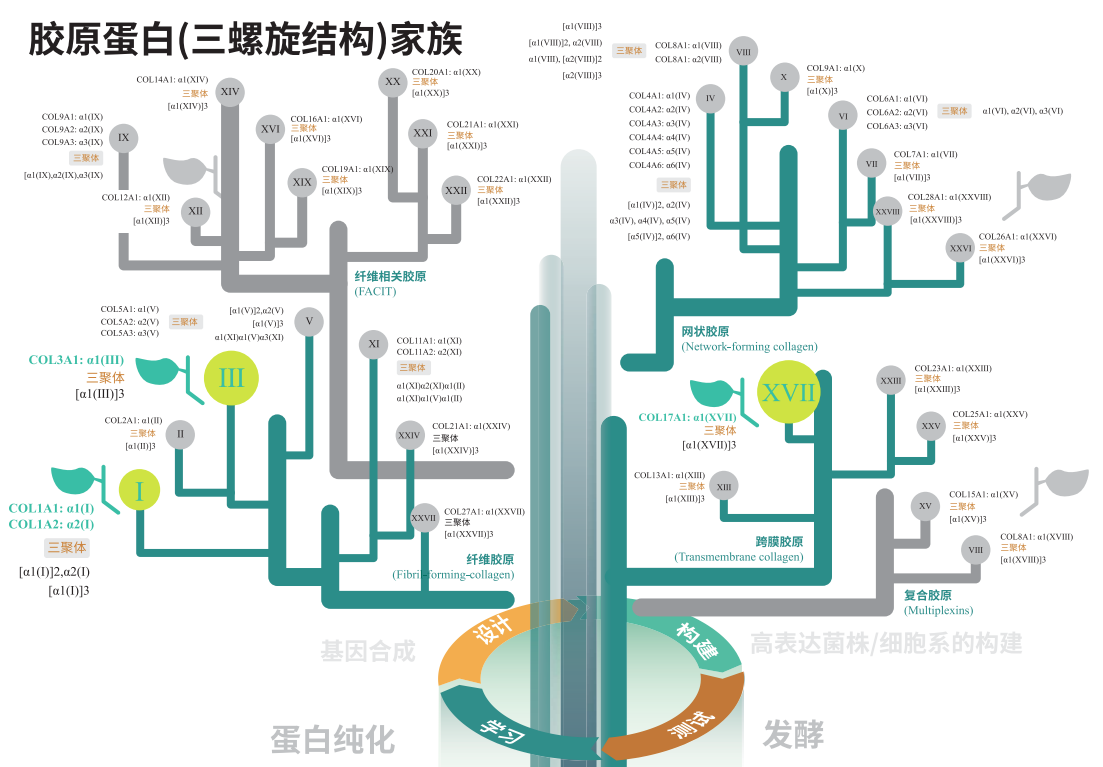
通过生物制造的方式获得高产量的重组胶原蛋白,极大满足了现今市场上胶原蛋白需求供不应求的缺口。
基因工程重组胶原蛋白是将人体胶原蛋白基因进行特定序列设计、酶切和拼接、连接载体后转入宿主细胞内,包括微生物、动物和植物等,再进行发酵诱导表达生产的胶原蛋白或类似物的技术。相比传统动物提取方式,生物制造重组胶原蛋白在原料来源、生物相容性、生产效率和成本,以及环境影响等方面都具有显著的优势。
随着国家政策、产业及资本对重组胶原蛋白领域的聚焦,合成生物学技术成为重组胶原蛋白研发的制胜法宝。目前,部分类型的重组胶原蛋白已成功进行商业化开发与生产,各类相关研究也在日趋深入。生物制造突破传统生产方式的局限,是推动经济增长和产业升级的重要力量,未来潜力无限。
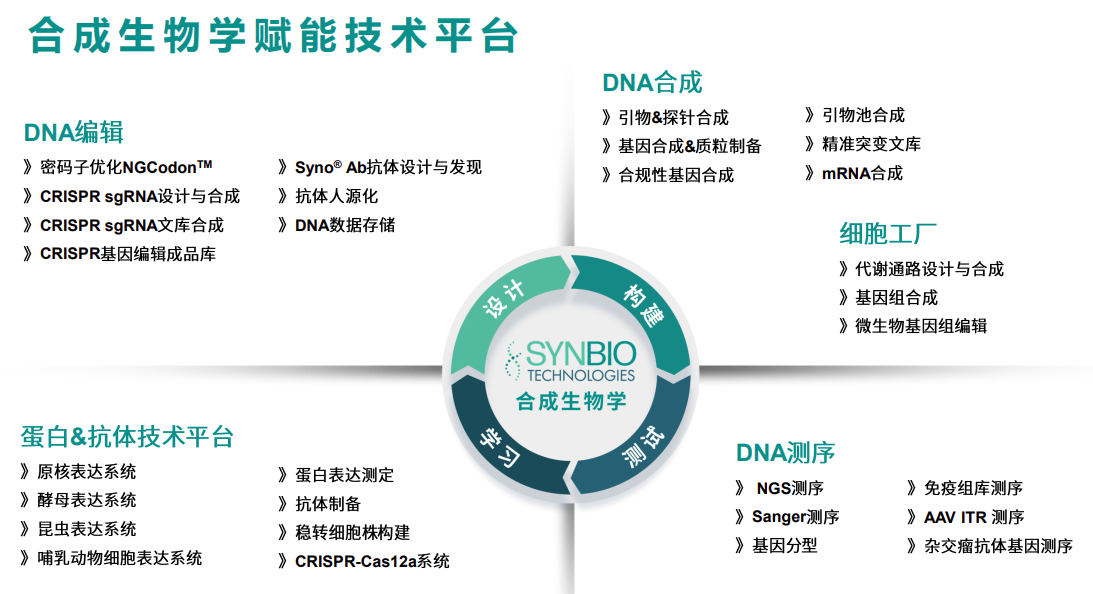
泓迅生物“新质生产力”——合成生物学赋能技术平台
泓迅生物已成功搭建全面的合成生物学赋能技术平台。通过DBTL(设计-构建-测试-学习)循环过程,能成功构建特定需求的稳转细胞株,生产出符合市场需求的产品,赋能下游应用开发进程及商业化落地。
泓迅生物在“新质生产力”的驱动下,探索新的研发方向和技术创新,为重组胶原蛋白开发应用创造更多可能! 先进的设计与制造为您提供医美活性成分AAI胶原蛋白合成生物学解决方案。

未来展望
目前,微生物细胞工厂的构建与优化仍存在着许多挑战。微生物目标合成途径的强化会受到细胞本身复杂的代谢调控网络的限制;另一方面,工业发酵环境通常包括高温、氧化、pH波动、高渗透压、有机溶剂、重金属等因素,严重影响微生物的生长和生产。
基因底层技术结合“DBTL”策略对代谢途径进行动态调控使目标产物的产量最大化,提高生物制造过程的智能性,是优化微生物细胞工厂的一致方向。合成生物学作为推动生物制造领域革新的重要引擎,正引领着行业向着更高、更远的领域迈进。
期待在新质生产力的加持下,实现从生物制造到生物智造的跨越,促进我们在技术创新、成本降低和效率提升等方面的全面进步。
References
[1] Zhang YP, Sun J, Ma Y. Biomanufacturing: history and perspective. J Ind Microbiol Biotechnol. 2017 May;44(4-5):773-784. doi: 10.1007/s10295-016-1863-2. Epub 2016 Nov 11. PMID: 27837351.
[2] Ro D K, Paradise E M, Ouellet M, et al. Production of the antimalarial drug precursor artemisinic acid in engineered yeast[J]. Nature, 2006, 440(7086): 940-943.
[3] 秦磊,俞杰,宁小钰,等.合成生物系统构建与绿色生物“智”造[J].化工学bao报,2020,71(09):3979-3994
[4] 石婷,宋展,宋世怡,等.体外生物转化(in vitro BioTransformation,ivBT):生物制造的新前沿[J/OL].合成生物学,1-24[2024-05-27].
声明:本网转发此文章,旨在为读者提供更多信息资讯,所涉内容不构成投资、消费建议。文章事实如有疑问,请与有关方核实,文章观点非本网观点,仅供读者参考。
- 上一篇:
陕西省老医协生殖医学医院靠谱吗 - 下一篇:
返回列表
延伸阅读
- 陕西省老医协生殖医学医院靠谱吗2024-06-18
- 法医界专家齐聚杭州,共话虚拟解剖未来发展2024-06-18
- 首家“配方研究所”成立,口服抗衰迈入硬核功效时代2024-06-17
- 国家人类基因组基因与生物工程联合实验室暨 诺赛国际医学研究院湖北分院“两库一室” 第一期工程签约正式落户咸宁2024-06-14
- 扬子江药业集团迎来集团第十个“安全环保月”,彰显绿色发展决心2024-06-14
- 长寿蛋白Sirtuin激活新方式!BECHI细胞小金盒创新引入新一代专利核糖素2024-06-14
编辑推荐
-
公益问诊:4月21日,名医列席CMTF医旅展,为不孕...
2023-03-17
-
西安:防疫升级后的市民生活...
2022-01-10
-
西安:优化诊疗流程 确保患者顺利就医...
2022-01-10
-
想要补肾应该吃什么 常吃这些食物让你肾越来越好...
2022-01-10
-
章鱼与鱿鱼的区别有哪些 简单一招便可分辨它们...
2022-01-10




